Die Fähigkeit des Menschen, Knochen stetig zu erneuern und somit widerstandsfähig zu halten, nimmt mit zunehmendem Alter ab und wird durch Krankheiten wie Osteoporose weiter eingeschränkt. Um der alternden Bevölkerung zu helfen, suchen Forscherinnen und Forscher nach neuen Therapien zur Verbesserung der Knochenregeneration. Ein interdisziplinäres Team des Biotechnologischen Zentrums (BIOTEC), der Medizinischen Fakultät und des Max-Bergmann-Centrums für Biomaterialien (MBC) der TU Dresden hat nun neuartige bioinspirierte Moleküle entwickelt, welche die Knochenregeneration bei Mäusen verbessern. Die Ergebnisse wurden in der Fachzeitschrift Biomaterials veröffentlicht. Diese Moleküle basieren auf Glykosaminoglykanen, langkettigen Zuckern wie Hyaluronsäure oder Heparin. Sie können in Biomaterialien eingebunden und somit lokal in Knochendefekte eingebracht werden.
Eine süße Lösung als Knochenheilungsturbo
„Dank der Arbeit unserer Gruppe und anderer Gruppen kennen wir einen bestimmten molekularen Weg, den Wnt-Signalweg, der die Knochenbildung und -reparatur reguliert. Wir konnten ihn auf zwei Bremssignale eingrenzen, die gemeinsam die Knochenregeneration blockieren: Sclerostin und Dickkopf-1“, erklärt Prof. Lorenz Hofbauer. „Die große Herausforderung für die Entwicklung von Medikamenten zur Verbesserung der Knochenheilung, besteht darin, diese beiden Blockade-Proteine gleichzeitig und effizient auszuschalten.“
Ein interdisziplinärer Ansatz war der Schlüssel zum Erfolg. Die Gruppe Strukturelle Bioinformatik unter der Leitung von Prof. Maria Teresa Pisabarro am Biotechnologischen Zentrum (BIOTEC) der TU Dresden und die Gruppe Funktionelle Biomaterialien von PD Dr. Vera Hintze vom Max-Bergmann-Zentrum für Biomaterialien, Institut für Werkstoffwissenschaft bündelten ihre Expertise mit dem Knochenexperten Hofbauer von der Medizinischen Fakultät der TU Dresden.
Knochenheilung um 50 Prozent gesteigert
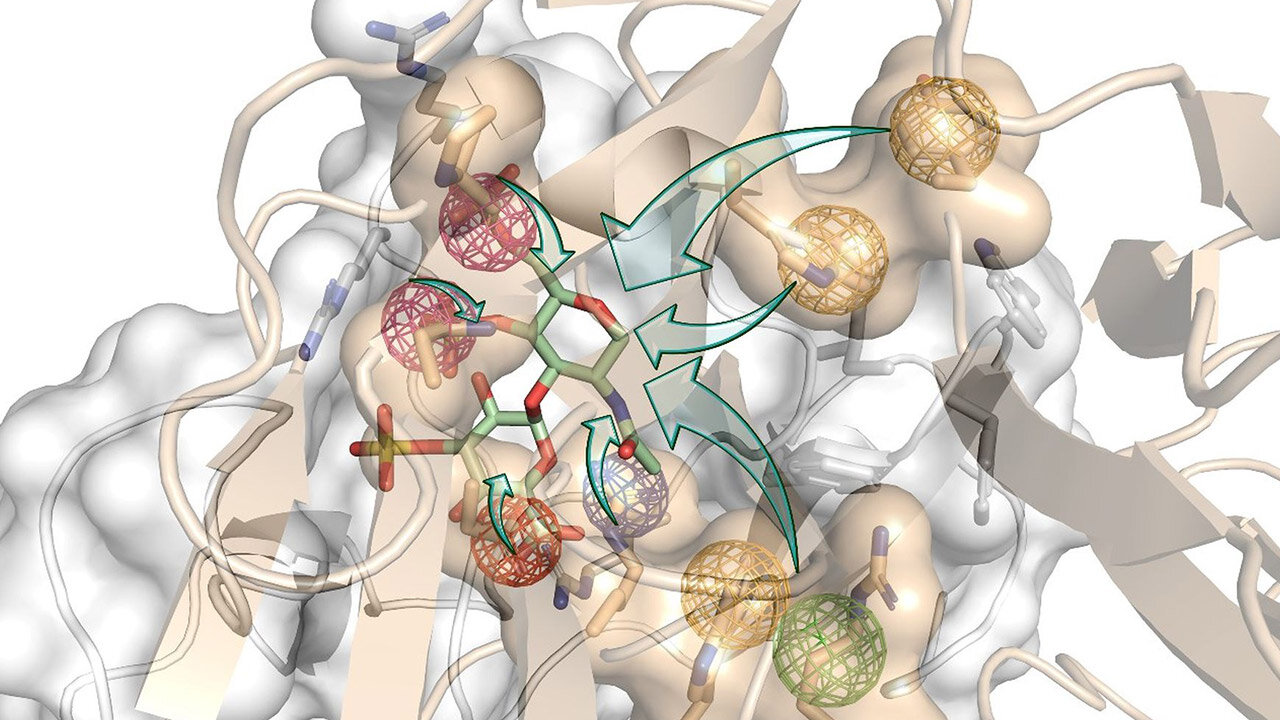
„Seit mehreren Jahren nutzen wir die Möglichkeiten der Computersimulation, um zu untersuchen, wie Proteine, welche die Knochenbildung regulieren, mit ihren Rezeptoren interagieren. All dies mit dem Ziel, neuartige Moleküle zu entwerfen, welche diese Interaktionen gezielt beeinflussen können. Wir arbeiteten im Tandem zwischen Computer und Labor, entwarfen und testeten neuartige Moleküle, übertrugen die Ergebnisse auf unsere molekularen Modelle und lernten mehr über die molekularen Eigenschaften, die für unser Ziel erforderlich waren“, erklärt Prof. Pisabarro.
Das Team von Prof. Hofbauers Bone Lab setzte schließlich mit diesen Molekülen beladene Biomaterialien bei Knochendefekten in Mäusen ein, um ihre Wirksamkeit zu testen. Dabei erwiesen sich die mit den neuen Molekülen beladenen Materialien im Vergleich zum Standard-Biomaterial als deutlich wirksamer und steigerten die Knochenheilung um bis zu 50 Prozent, was auf ein enormes regeneratives Potenzial hinweist.
Wertschöpfungskette: Vom Computer ins Labor und zurück
Das multidisziplinäre Team nutzte rationales Wirkstoffdesign, um neuartige Moleküle mit maßgeschneiderten Eigenschaften und minimalen Nebenwirkungen zu entwickeln. Durch den Einsatz von Berechnungsmethoden zur Vorhersage und Verfeinerung der Eigenschaften der entworfenen Moleküle konnte das Team eine Reihe von Kandidaten entwickeln, die das größte Potenzial haben, die Proteine auszuschalten, und die Knochenregeneration zu blockieren.
Originalveröffentlichung:
Ruiz-Gómez G, Salbach-Hirsch J, Dürig JN, Köhler L, Balamurugan K, Rother S, Heidig SL, Moeller S, Schnabelrauch M, Furesi G, Pählig S, Guillem-Gloria PM, Hofbauer C, Hintze V, Pisabarro MT, Rademann J, Hofbauer LC: Rational engineering of glycosaminoglycan-based Dickkopf-1 scavengers to improve bone regeneration. Biomaterials (April 2023) https://doi.org/10.1016/j.biomaterials.2023.122105
Die Expertise der Gruppe Pisabarro ermöglichte eine detaillierte Analyse der 3-D-Strukturen der beiden Proteine, die die Knochenregeneration blockieren. Auf diese Weise konnten sie die Interaktion der Proteine mit ihren Rezeptoren in 3-D modellieren und Schlüsselstrukturen identifizieren, das heißt, spezifische physikalisch-chemische und dynamische Eigenschaften, die für die biologische Interaktion wesentlich sind. „Mit Hilfe von Molecular Modelling haben wir neue Strukturen entworfen, welche die relevanten Rezeptorinteraktionen mit den beiden Proteinen nachahmen. Wir wollten, dass diese Bindung stärker ist als ihre natürlichen Wechselwirkungen. Auf diese Weise würden unsere neuen Moleküle die Proteine einfangen und effektiv ausschalten und dadurch die Knochenregeneration fördern“, erklärt Pisabarro.
Auch ein Schritt hin zu weniger Tierversuchen
„Die von Prof. Pisabarros Gruppe entworfenen Moleküle wurden von unseren Kollegen an der Freien Universität Berlin synthetisiert und dann von uns in Bezug auf ihre Proteinbindungseigenschaften mittels biophysikalischer Interaktionsanalyse untersucht ", sagt Dr. Hintze. „Für jedes Molekül konnten wir messen, wie stark es an die Proteine bindet sowie mit der Bindung der Proteine an ihre natürlichen Rezeptoren interferiert. Auf diese Weise konnten wir empirisch zeigen, wie effektiv sie damit die hemmenden Proteine ausschalten. Die biologische Relevanz dieser Wechselwirkungsstudien testete Hofbauers Gruppe in einem Zellkulturmodell und später in Mäusen.“ Die Ergebnisse dieser iterativen Tests sind von großem Wert, um die derzeitigen molekularen Modelle der Pisabarro-Gruppe zu verbessern und als Blaupause für die Entwicklung neuartiger und besserer Moleküle in der Zukunft zu dienen. Ein solcher Ansatz stellt auch sicher, dass Tierversuche auf ein Minimum reduziert werden und erst in der Endphase des Projekts zum Einsatz kommen.

Auf dem Weg zur Arzneimittelentwicklung
Die Ergebnisse des Teams stellen einen aufregenden Schritt mit beträchtlicher klinischer Relevanz dar. Die neu entwickelten Moleküle könnten dazu verwendet werden, Proteine auszuschalten, die die Knochenregeneration blockieren, und zur Entwicklung neuer, wirksamerer Therapien für Knochenbrüche und andere Knochenerkrankungen führen. Das Team setzt seine erfolgreiche Zusammenarbeit fort. „Wir beantragen die Finanzierung einer präklinischen Studie, um diese Moleküle als innovative Therapie für eine Studie an Menschen weiterzuentwickeln“, so Hofbauer.